Asam urat, suatu bentuk artritis inflamasi yang umum, muncul dari pengendapan kristal monosodium urat di persendian akibat hiperurisemia kronis. Monoterapi farmakologis saat ini seperti inhibitor xantin oksidase, urikosurik, NSAID, kortikosteroid, dan kolkisin seringkali terbatas oleh efikasi aksi ganda yang tidak memadai, bioavailabilitas yang suboptimal, dan efek samping sistemik. Sistem penghantaran obat berbasis nanocarrier yang sedang berkembang menawarkan alternatif yang menjanjikan dengan meningkatkan farmakokinetik dan meningkatkan penghantaran yang ditargetkan ke jaringan yang meradang. Meskipun ko-enkapsulasi beberapa terapi masih kurang dieksplorasi pada asam urat, kemajuan dalam penyakit inflamasi terkait mendukung aplikasinya di masa depan. Tinjauan ini mengeksplorasi keterbatasan terapi asam urat konvensional dan menyoroti kemajuan terkini dalam teknologi nanocarrier, termasuk liposom, niosom, dan etosom, untuk memberikan agen antiinflamasi dan penurun asam urat. Perhatian khusus diberikan pada strategi fungsionalisasi yang memungkinkan penghantaran spesifik lokasi dan pelepasan obat berurutan, terutama dalam lingkungan mikro asam dan oksidatif yang menjadi ciri khas serangan gout akut. Pemberian bersama agen seperti alopurinol atau febuxostat dengan NSAID atau kortikosteroid dapat mengurangi beban pil, meningkatkan sinergi terapeutik, dan meningkatkan kepatuhan pasien. Meskipun translasi klinis masih dalam tahap awal, rasional mekanistik dan hasil praklinis yang menggembirakan dari nanocarrier yang responsif dan terfungsional menggarisbawahi potensinya untuk memajukan pengobatan presisi dalam manajemen gout.
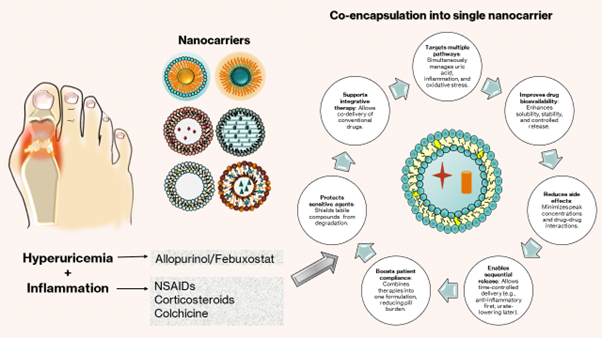
Gout adalah bentuk artritis inflamasi yang paling umum, ditandai dengan episode nyeri sendi yang hebat, kemerahan, dan pembengkakan. Kondisi ini melibatkan artropati terkait kristal yang disebabkan oleh akumulasi monosodium urat di sendi sinovial. Hal ini terkait dengan hiperurisemia akibat perubahan jalur metabolisme purin. Gout adalah gangguan metabolisme yang ditandai dengan artritis inflamasi berulang dan memiliki prevalensi global yang tinggi bersama dengan disabilitas fungsional yang signifikan. Prevalensi gout lebih tinggi pada pria dan meningkat seiring bertambahnya usia. Tanpa penanganan yang tepat, gout dapat menyebabkan kerusakan sendi kronis dan kekambuhan berulang serta telah dikaitkan dengan komorbiditas seperti komplikasi kardiovaskular dan ginjal. Faktor-faktor seperti predisposisi genetik, pengaruh lingkungan, dan pilihan gaya hidup tidak sehat, termasuk diet tinggi purin dan konsumsi alkohol berlebihan, dapat berkontribusi pada perkembangan asam urat.
Peningkatan kadar asam urat serum (sUA) yang terus-menerus di atas ambang batas kelarutan (>6,8 mg/dL) mendorong pengendapan kristal monosodium urat di jaringan lunak dan persendian, yang menyebabkan peradangan dan secara bertahap merusak persendian. Oleh karena itu, mengurangi kadar sUA hingga kurang dari 6 mg/dL merupakan tujuan utama pengobatan asam urat karena membantu melarutkan endapan yang sudah ada dan menghambat pembentukan kristal baru. Gout pada peradangan dimulai ketika kristal MSU menstimulasi sistem imun bawaan melalui reseptor Toll-like (TLR) dan protein 3 yang mengandung domain NOD-, LRR-, dan pirin (NLRP3) inflammasom, yang mengakibatkan sekresi sitokin inflamasi termasuk interleukin-6 (IL-6), interleukin-1 beta (IL-1β), faktor nekrosis tumor-alfa (TNF-α), dan interleukin-8 (IL-8). Sitokin memulai jalur pensinyalan inflamasi hilir, seperti jalur Janus kinase/transducer sinyal dan aktivator transkripsi (JAK/STAT), mitogen-activated protein kinase (MAPK), dan phosphatidylinositol 3-kinase/protein kinase B (PI3K/Akt) yang mengakibatkan aktivasi ekspresi gen inflamasi. Interleukin 6 (IL-6) memfasilitasi perekrutan sel imun dan memperburuk peradangan lokal, sehingga memperparah kondisi daripada meredakannya. Peningkatan kadar IL-6 secara klinis dikaitkan dengan tofi gout, deformitas sendi, dan peningkatan risiko penyakit kardiovaskular. Dalam keadaan normal, pensinyalan IL-6 dimodulasi oleh protein termasuk penekan pensinyalan sitokin 1 dan 3 (SOCS1 dan SOCS3) dan fosfatase yang mengandung domain daerah homologi Src 2 (SHP1). Namun, pada gout, mekanisme pengaturan ini sering kali dilampaui, yang menyebabkan peradangan yang terus-menerus. Beberapa strategi terapeutik telah dikembangkan untuk mengelola asam urat berdasarkan jalur ini.Terapi anti-hiperurisemik kontemporer berfokus pada penurunan konsentrasi urat serum dengan mengatasi produksi, ekskresi, dan degradasi asam urat. Agen farmakologis yang umum digunakan meliputi penghambat xantin oksidase (XO), termasuk allopurinol (lini pertama) dan febuxostat; urikosurik seperti benzbromarone, probenecid, sulfinpyrazone, lesinurad, dan urikase rekombinan pegloticase. Urikosurik, meskipun efektif, meningkatkan beban pada ginjal dan meningkatkan kemungkinan pembentukan batu ginjal, sehingga tidak tepat untuk pasien dengan penyakit ginjal kronis (CKD) berat (Dehlin et al., 2020). Obat antiinflamasi nonsteroid (NSAID), glukokortikosteroid, dan kolkisin umumnya digunakan untuk penanganan asam urat akut guna meredakan nyeri dan peradangan. Namun, obat-obatan ini dikaitkan dengan efek samping yang cukup besar dan potensi interaksi obat, terutama pada pasien lanjut usia atau individu dengan penyakit ginjal kronis (CKD) atau diabetes. Alternatif terbaru yang menargetkan IL-1β, termasuk canakinumab, anakinra, dan rilonacept, menunjukkan efek antiinflamasi yang signifikan. Meskipun demikian, aplikasinya dalam pengobatan asam urat masih terbatas, karena canakinumab telah mendapat persetujuan dari Badan Obat-obatan Eropa (EMA) tetapi belum dari Badan Pengawas Obat dan Makanan (FDA)
Keyword : Gout, monosodium urate, nanocarrier, niosomes, anti-inflammatory, allopurinol